Radiology(IF=15.2)中南大学湘雅二医院肖煜东教授等团队:基于CT放射组学的机器学习识别肝细胞癌瘤内纤维化及其潜在血管生成
news2026/5/15 6:55:48
01文献学习今天分享的文献是由中南大学湘雅二医院肖煜东教授等团队于2026年5月在放射学领域顶刊《Radiology》中科院1区topIF15.2上发表的研究“CT Radiomics-based Machine Learning to Identify Intratumoral Fibrosis and Underlying Angiogenesis in Hepatocellular Carcinoma”即基于CT放射组学的机器学习识别肝细胞癌瘤内纤维化及其潜在血管生成该研究开发并验证了一种基于CT影像的放射组学模型Rad-ITF评分用于无创性评估肝细胞癌HCC中的瘤内纤维化ITF分级。研究发现高Rad-ITF评分的HCC患者在接受TACE治疗后预后更差进展生存期更短、应答率更低并且肿瘤组织中血管生成相关基因表达显著上调。该模型在多个独立队列中表现出良好的诊断性能AUC最高达0.86并具有作为TACE联合抗血管生成治疗筛选工具的潜力。创新点①首次构建CT影像组学模型无创识别HCC瘤内纤维化ITF等级替代有创病理活检实现术前精准分级。②揭示高ITF等级与血管生成通路VEGFR3/PDGFRA上调的分子关联通过多组学及空间转录组验证。③建立XGBoost模型Rad-ITF评分同时预测ITF及TACE预后整合了影像、病理、转录组与临床结局。临床价值①避免术前活检风险利用常规CT影像即可评估ITF为无法/不愿穿刺的HCC患者提供决策依据。②优化TACE治疗分层高Rad-ITF评分患者疗效差、PFS短提示应联合抗血管生成药物或调整方案。③筛选抗血管生成治疗优势人群高评分组血管生成基因高表达指导TACE靶向联合治疗策略提高个体化精准度。02研究背景和目的研究背景肝细胞癌HCC是一种高度异质性的恶性肿瘤其复杂的肿瘤微环境对疾病进展和治疗响应具有重要影响。瘤内纤维化ITF是细胞外基质重塑所导致的组织学改变在实体瘤中可见但在HCC中相对少见。然而部分HCC亚型如硬癌样亚型可表现为高ITF等级并与不良预后密切相关。目前经动脉化疗栓塞术TACE是中期HCC的一线治疗方案但其疗效仍不理想。这可能与ITF形成的物理屏障有关致密的细胞外基质沉积、增加的基质硬度、降低的血管通透性以及升高的间质流体压力共同阻碍了栓塞剂和化疗药物的有效递送。此外新近证据表明ITF还可能促进肿瘤血管生成进而影响抗血管生成治疗的疗效。鉴于ITF在预后判断和治疗指导中的潜在重要意义术前无创评估ITF等级显得尤为关键。然而常规HCC诊断流程中并不包括全面的组织学评估且传统影像特征如靶样外观的解读存在显著的观察者间变异性κ值仅为0.20–0.61。影像组学作为一种新兴的无创方法能够定量提取高维度图像特征反映潜在的肿瘤病理生理特征有望成为替代性生物标志物。但迄今为止基于CT影像组学进行ITF分级及其与TACE预后关联的研究仍十分有限亟需深入探索。研究目的本研究旨在开发并验证一个基于CT影像组学的机器学习模型用于术前无创地分类肝细胞癌HCC中的瘤内纤维化ITF等级并进一步评估该模型所判定的ITF分级与接受TACE治疗的HCC患者预后以及肿瘤血管生成水平之间的关联。具体而言研究团队首先利用多中心回顾性与前瞻性队列以组织病理学Sirius红染色和HE染色为金标准将患者分为低ITF等级与高ITF等级通过特征提取与筛选构建了XGBoost模型即Rad-ITF评分并在内部和外部验证集中验证其诊断效能。其次在结局测试队列中根据Rad-ITF评分将接受TACE的中期HCC患者分为高低两组比较两组间的无进展生存期PFS和肿瘤缓解率以评估模型对治疗结局的预测价值。最后利用TCGA公共数据库及前瞻性收集的基因组测试队列通过RNA测序、单细胞RNA测序和空间转录组学分析比较高低Rad-ITF评分组间血管生成相关基因表达、内皮细胞及成纤维细胞浸润水平并定量分析微血管密度MVD从而验证Rad-ITF评分与血管生成水平的相关性为后续联合TACE与抗血管生成治疗提供理论依据。03数据和方法研究数据总样本量1675例HCC患者1406男269女多中心队列训练集653例内部验证集371例外部验证集173例结局测试集427例接受TACE的中期HCCTCGA测试集39例CT RNA-seq基因组测试集12例前瞻性单细胞RNA-seq 空间转录组病理金标准Sirius red 和 HE 染色评估ITF分级图 1研究流程图技术方法影像组学从动脉期和门静脉期CT中提取3668个特征筛选出17个用于建模。机器学习模型XGBoost最优模型输出Rad-ITF评分。预后分析Kaplan-Meier、Cox回归、倾向评分匹配PSM、逆概率加权IPTW。分子分析TCGA血管生成相关基因表达单细胞RNA-seq 空间转录组细胞类型富集、基因空间定位免疫组化CD34染色评估微血管密度MVD04实验结果模型性能训练集AUC0.86内部验证集AUC0.85外部验证集AUC0.82预后价值高Rad-ITF评分组肿瘤应答率更低46.2% vs 62.0%PFS更差6.8月 vs 11.2月P 0.001血管生成关联高Rad-ITF评分组中VEGFR3、PDGFRA等基因表达显著上调内皮细胞和成纤维细胞富集MVD显著升高55.0 vs 45.0P 0.001图 2低/高ITF分级的CT图像分割与病理染色示例该图展示了低ITF与高ITF肝细胞癌HCC的CT图像、肿瘤分割掩模及Sirius红染色。A-B为41岁男性患者瘤径46 mm的动脉期和门静脉期轴位CTC-D分别用红色和绿色掩模标注了动脉期与门静脉期的肿瘤轮廓E-F为对应病理图像低ITF组E显示稀疏胶原纤维而高ITF组F呈现密集的红色胶原沉积。该图直观体现了放射组学特征提取的基础以及ITF分级的组织学参考标准。图 3Rad-ITF评分模型的诊断性能对比该图评估了放射组学模型仅Rad-ITF评分与综合模型联合肝硬化的效能。A-C为ROC曲线在训练、内部验证、外部验证队列中放射组学模型的AUC分别为0.86、0.85和0.82与综合模型无显著差异P均0.05。D-F决策曲线显示在较宽阈值概率范围内Rad-ITF评分的净获益优于“全治疗”或“不治疗”策略。G-H校准曲线表明预测概率与实际观测概率高度一致证实模型具有良好的校准度和临床实用性。图 4Rad-ITF评分与TACE预后关系的生存曲线及响应率该图比较了高低Rad-ITF评分组患者的无进展生存期PFS和肿瘤缓解率。A-C为Kaplan-Meier曲线高评分组中位PFS显著劣于低评分组原始队列6.8月 vs 11.2月P0.001经倾向评分匹配PSM和逆概率处理加权IPTW后差异依然显著。D-F条形图显示高评分组的客观缓解率ORR在匹配前后均低于低评分组如匹配前46.2% vs 62.0%P0.002。结果提示高Rad-ITF评分预示TACE疗效更差、进展更快。图 5Rad-ITF评分与血管生成水平的多组学关联分析该图通过单细胞测序和空间转录组揭示高Rad-ITF评分与血管生成上调的关系。A-B小提琴图显示高评分组中VEGFR3、VEGFR1、KDR、PDGFRA等基因表达显著升高校正P0.04。C-E展示内皮细胞和成纤维细胞在高评分组中显著富集校正P分别为0.02和0.03。F-H空间转录组定位显示VEGFR3和PDGFRA高表达集中于高纤维化区域低评分肿瘤I-J则几乎无表达。该图从分子和细胞层面证实Rad-ITF评分可作为血管生成的替代标志物。图 6Rad-ITF评分与微血管密度MVD的组织学验证该图通过CD34免疫组化染色验证高Rad-ITF评分与血管生成增加的相关性。A和B分别为低、高Rad-ITF评分HCC的代表性CD34染色图像200×高评分组显示更密集的微血管网络。C图解了MVD计数方法——在热点区域内手动标记并计数微血管示例中标记14条。D箱线图汇总了三个验证队列共715例低评分与482例高评分的MVD数据高评分组中位MVD为55.0IQR 44.0-68.0显著高于低评分组的45.0IQR 33.0-59.0P0.001。该图为Rad-ITF评分反映肿瘤血管生成水平提供了直接病理学证据。05研究结论该研究基于CT放射组学构建了名为Rad-ITF评分的机器学习模型用于术前无创评估肝细胞癌HCC的瘤内纤维化ITF等级。研究在多个独立队列中验证了该模型的诊断性能训练、内部验证和外部验证队列的AUC分别达到0.86、0.85和0.82显著优于传统影像特征如靶样外观。进一步分析表明高Rad-ITF评分与更差的TACE治疗反应和更短的无进展生存期PFS显著相关提示其在预后分层中的价值。此外研究还发现高Rad-ITF评分组中血管生成相关基因如VEGFR3、PDGFRA表达上调内皮细胞和成纤维细胞浸润增加微血管密度升高表明该评分能间接反映肿瘤的血管生成水平。综上Rad-ITF评分不仅可作为HCC中ITF等级的有效替代标志物还能为TACE疗效预测和联合抗血管生成治疗策略的制定提供理论依据。06QAQ1什么是Rad-ITF评分A1Rad-ITF评分是一种基于CT影像的放射组学机器学习模型采用XGBoost算法构建。研究从动脉期和门静脉期CT图像中提取3668个特征最终筛选出17个关键特征用于计算该评分用于无创性区分肝细胞癌HCC的瘤内纤维化ITF高分级与低分级病理金标准为Sirius red染色。Q2Rad-ITF评分与接受TACE治疗的中期HCC患者的预后有何关联A2在包含427例接受TACE治疗的中期HCC患者的结局测试队列中高Rad-ITF评分≥0.34与显著更差的预后相关①肿瘤应答率高评分组为46.2%66/143低评分组为62.0%176/284P0.002②中位无进展生存期PFS高评分组为6.8个月95% CI: 5.4, 8.3低评分组为11.2个月95% CI: 10.4, 12.3P0.001经倾向评分匹配PSM和逆概率加权IPTW校正后上述差异仍然显著。提示Rad-ITF评分可作为TACE术前预后分层的有力工具。Q3高Rad-ITF评分与HCC肿瘤血管生成水平之间存在怎样的关联A3多组学分析一致表明高Rad-ITF评分与更高的肿瘤血管生成活性显著相关①基因表达层面TCGA队列n39高评分组中VEGFR3等血管生成相关基因表达显著上调adjusted P0.04。②单细胞RNA测序前瞻性队列n12高评分组中内皮细胞adjusted P0.02和成纤维细胞adjusted P0.03显著富集且VEGFR3、PDGFRA等基因表达升高。③空间转录组2例VEGFR3和PDGFRA主要表达于高纤维化区域。④组织学验证全体训练验证集高评分组的微血管密度MVDCD34染色中位数为55.0显著高于低评分组的45.0P0.001。这些结果表明Rad-ITF评分可间接反映HCC的血管生成状态为联合抗血管生成治疗提供理论依据。参考文献Wang TC, Wei N, Bao Y, Li JX, Zhou P, Sun Y, Wang LZ, Cai WW, Chang DH, Xiao YD. CT Radiomics-based Machine Learning to Identify Intratumoral Fibrosis and Underlying Angiogenesis in Hepatocellular Carcinoma. Radiology. 2026 May;319(2):e250736. doi: 10.1148/radiol.250736.
本文来自互联网用户投稿,该文观点仅代表作者本人,不代表本站立场。本站仅提供信息存储空间服务,不拥有所有权,不承担相关法律责任。如若转载,请注明出处:http://www.coloradmin.cn/o/2614463.html
如若内容造成侵权/违法违规/事实不符,请联系多彩编程网进行投诉反馈,一经查实,立即删除!相关文章
SpringBoot-17-MyBatis动态SQL标签之常用标签
文章目录 1 代码1.1 实体User.java1.2 接口UserMapper.java1.3 映射UserMapper.xml1.3.1 标签if1.3.2 标签if和where1.3.3 标签choose和when和otherwise1.4 UserController.java2 常用动态SQL标签2.1 标签set2.1.1 UserMapper.java2.1.2 UserMapper.xml2.1.3 UserController.ja…
wordpress后台更新后 前端没变化的解决方法
使用siteground主机的wordpress网站,会出现更新了网站内容和修改了php模板文件、js文件、css文件、图片文件后,网站没有变化的情况。
不熟悉siteground主机的新手,遇到这个问题,就很抓狂,明明是哪都没操作错误&#x…
网络编程(Modbus进阶)
思维导图 Modbus RTU(先学一点理论)
概念 Modbus RTU 是工业自动化领域 最广泛应用的串行通信协议,由 Modicon 公司(现施耐德电气)于 1979 年推出。它以 高效率、强健性、易实现的特点成为工业控制系统的通信标准。 包…
UE5 学习系列(二)用户操作界面及介绍
这篇博客是 UE5 学习系列博客的第二篇,在第一篇的基础上展开这篇内容。博客参考的 B 站视频资料和第一篇的链接如下:
【Note】:如果你已经完成安装等操作,可以只执行第一篇博客中 2. 新建一个空白游戏项目 章节操作,重…
IDEA运行Tomcat出现乱码问题解决汇总
最近正值期末周,有很多同学在写期末Java web作业时,运行tomcat出现乱码问题,经过多次解决与研究,我做了如下整理:
原因:
IDEA本身编码与tomcat的编码与Windows编码不同导致,Windows 系统控制台…
利用最小二乘法找圆心和半径
#include <iostream>
#include <vector>
#include <cmath>
#include <Eigen/Dense> // 需安装Eigen库用于矩阵运算 // 定义点结构
struct Point { double x, y; Point(double x_, double y_) : x(x_), y(y_) {}
}; // 最小二乘法求圆心和半径 …
使用docker在3台服务器上搭建基于redis 6.x的一主两从三台均是哨兵模式
一、环境及版本说明
如果服务器已经安装了docker,则忽略此步骤,如果没有安装,则可以按照一下方式安装: 1. 在线安装(有互联网环境): 请看我这篇文章 传送阵>> 点我查看 2. 离线安装(内网环境):请看我这篇文章 传送阵>> 点我查看
说明:假设每台服务器已…
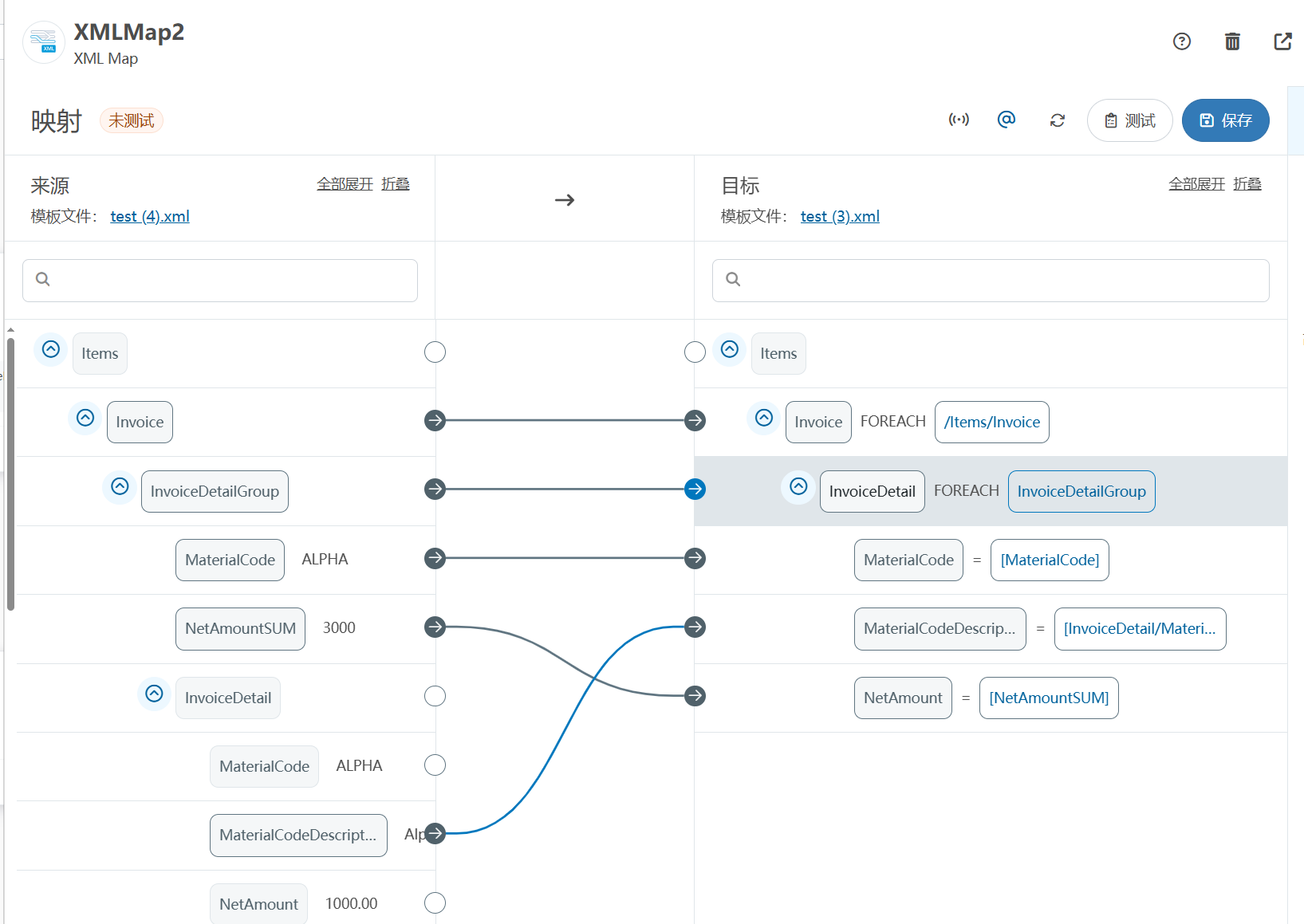
XML Group端口详解
在XML数据映射过程中,经常需要对数据进行分组聚合操作。例如,当处理包含多个物料明细的XML文件时,可能需要将相同物料号的明细归为一组,或对相同物料号的数量进行求和计算。传统实现方式通常需要编写脚本代码,增加了开…
LBE-LEX系列工业语音播放器|预警播报器|喇叭蜂鸣器的上位机配置操作说明
LBE-LEX系列工业语音播放器|预警播报器|喇叭蜂鸣器专为工业环境精心打造,完美适配AGV和无人叉车。同时,集成以太网与语音合成技术,为各类高级系统(如MES、调度系统、库位管理、立库等)提供高效便捷的语音交互体验。
L…
(LeetCode 每日一题) 3442. 奇偶频次间的最大差值 I (哈希、字符串)
题目:3442. 奇偶频次间的最大差值 I 思路 :哈希,时间复杂度0(n)。 用哈希表来记录每个字符串中字符的分布情况,哈希表这里用数组即可实现。
C版本:
class Solution {
public:int maxDifference(string s) {int a[26]…
【大模型RAG】拍照搜题技术架构速览:三层管道、两级检索、兜底大模型
摘要
拍照搜题系统采用“三层管道(多模态 OCR → 语义检索 → 答案渲染)、两级检索(倒排 BM25 向量 HNSW)并以大语言模型兜底”的整体框架: 多模态 OCR 层 将题目图片经过超分、去噪、倾斜校正后,分别用…
【Axure高保真原型】引导弹窗
今天和大家中分享引导弹窗的原型模板,载入页面后,会显示引导弹窗,适用于引导用户使用页面,点击完成后,会显示下一个引导弹窗,直至最后一个引导弹窗完成后进入首页。具体效果可以点击下方视频观看或打开下方…
接口测试中缓存处理策略
在接口测试中,缓存处理策略是一个关键环节,直接影响测试结果的准确性和可靠性。合理的缓存处理策略能够确保测试环境的一致性,避免因缓存数据导致的测试偏差。以下是接口测试中常见的缓存处理策略及其详细说明:
一、缓存处理的核…
龙虎榜——20250610
上证指数放量收阴线,个股多数下跌,盘中受消息影响大幅波动。 深证指数放量收阴线形成顶分型,指数短线有调整的需求,大概需要一两天。 2025年6月10日龙虎榜行业方向分析 1. 金融科技
代表标的:御银股份、雄帝科技
驱动…
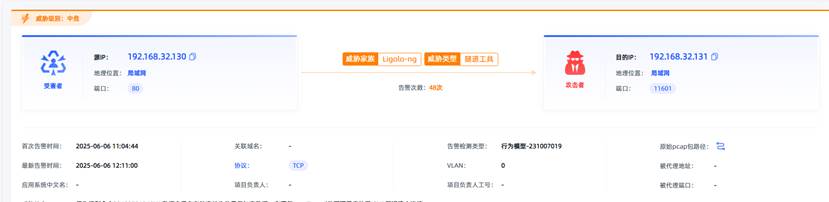
观成科技:隐蔽隧道工具Ligolo-ng加密流量分析
1.工具介绍
Ligolo-ng是一款由go编写的高效隧道工具,该工具基于TUN接口实现其功能,利用反向TCP/TLS连接建立一条隐蔽的通信信道,支持使用Let’s Encrypt自动生成证书。Ligolo-ng的通信隐蔽性体现在其支持多种连接方式,适应复杂网…
铭豹扩展坞 USB转网口 突然无法识别解决方法
当 USB 转网口扩展坞在一台笔记本上无法识别,但在其他电脑上正常工作时,问题通常出在笔记本自身或其与扩展坞的兼容性上。以下是系统化的定位思路和排查步骤,帮助你快速找到故障原因:
背景:
一个M-pard(铭豹)扩展坞的网卡突然无法识别了,扩展出来的三个USB接口正常。…
未来机器人的大脑:如何用神经网络模拟器实现更智能的决策?
编辑:陈萍萍的公主一点人工一点智能 未来机器人的大脑:如何用神经网络模拟器实现更智能的决策?RWM通过双自回归机制有效解决了复合误差、部分可观测性和随机动力学等关键挑战,在不依赖领域特定归纳偏见的条件下实现了卓越的预测准…
Linux应用开发之网络套接字编程(实例篇)
服务端与客户端单连接
服务端代码
#include <sys/socket.h>
#include <sys/types.h>
#include <netinet/in.h>
#include <stdio.h>
#include <stdlib.h>
#include <string.h>
#include <arpa/inet.h>
#include <pthread.h>
…
华为云AI开发平台ModelArts
华为云ModelArts:重塑AI开发流程的“智能引擎”与“创新加速器”!
在人工智能浪潮席卷全球的2025年,企业拥抱AI的意愿空前高涨,但技术门槛高、流程复杂、资源投入巨大的现实,却让许多创新构想止步于实验室。数据科学家…
深度学习在微纳光子学中的应用
深度学习在微纳光子学中的主要应用方向
深度学习与微纳光子学的结合主要集中在以下几个方向:
逆向设计 通过神经网络快速预测微纳结构的光学响应,替代传统耗时的数值模拟方法。例如设计超表面、光子晶体等结构。
特征提取与优化 从复杂的光学数据中自…